На что способны стволовые клетки: как повернуть жизнь вспять?
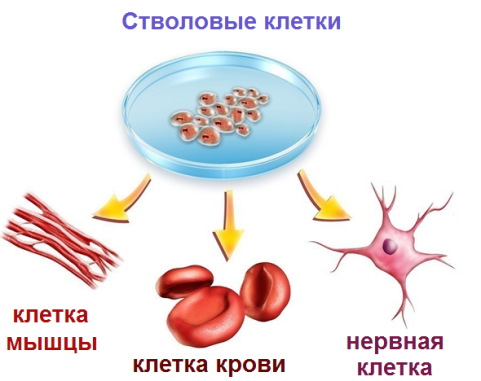 |
| Стволовые клетки дают начало всем клеткам организма — как от ствола дерева отходят все его ветви. Они — как младенцы: одна, когда вырастет, станет клеткой крови, а другая — нервной клеткой, и так далее |
Нобелевская премия за возможность начать сначала
Вплоть до XX века ученые полагали, что живая клетка — как человек: в детстве все дороги открыты, а после созревания и взросления обратного пути уже нет. Но в 2012 году Нобелевскую премию вручили ученым, которые перевернули это представление. Они доказали, что зрелые клетки могут быть «перепрограммированы» обратно в состояние юности и созреть заново, выбрав другую судьбу. Эту технологию перепрограммирования обозначают английской аббревиатурой iPSC (Induced pluripotent stem cell — индуцированные стволовые клетки). Она означает, что стволовые клетки не взяты готовыми (например, из эмбриона), а созданы из обычных клеток; а также то, что такая клетка может стать любой, какая только существует в человеческом организме — и быть использованной для лечения.
image002.png) |
| Как работают с технологией iPSC. Адаптировано из обзорной статьи австралийских ученых от 2020 года |
В статье о вакцине можно получить представление о том, какой многолетний путь проходит любой лекарственный препарат от создания до поступления в аптеки: сначала изучение в пробирках, потом на лабораторных животных и лишь затем, с большой осторожностью — на добровольцах.
Но как искать лекарства от болезней мозга? Ведь идея извлечь несколько клеток из человеческой головы даже не обсуждается. Но что если взять, скажем, волос человека, страдающего болезнью Паркинсона, и сделать из него модель мозга — модель заболевания — и подбирать лекарства не на лабораторных мышах, а на этой модели?
Волос + губка = сердце
Радует, когда ученые не замыкаются на своем предмете, а демонстрируют общую эрудицию. Так, строка из 47-го сонета Шекспира «У сердца с глазом тайный договор» стала эпиграфом к публикации итальянских исследователей о лечении болезней сердца с помощью стволовых клеток. Ученые брали образцы клеток у людей, болеющих мышечной дистрофией — и, используя технологию iPSС, моделировали ткань сердца каждого конкретного пациента (люди с этим заболеванием нередко погибают именно от сердечной недостаточности: другим мышцам организма можно помочь физкультурой или лекарствами — с сердцем же дело обстоит труднее). Ученые проводят попытки лечения этого генетического недуга как посредством iPSC, так и с использованием технологии CRISPR/Cas9.
Кроме того, в начале тысячелетия искали способ применения стволовых клеток для реабилитации людей после инфаркта миокарда. Медики обсуждали: что же такое стволовые клетки сердца — надежда или иллюзия? Проблема получила гласность в 1998 году, когда команда Пьеро Анверзы из Нью-Йорка заявила, что нашла в сердце стволовые клетки (до этого считалось, что в работе сердца участвуют только «взрослые» клетки). Через пять лет сотрудники Анверзы нашли способ «пометить» эти клетки, чтобы под микроскопом было видно именно их.
Идею подхватили во всем мире. Но, к сожалению, воссоздать опыты Анверзы не удавалось, и до сих пор идет расследование и судебный процесс: подозрение в подделке результатов по-прежнему не доказано, но и не опровергнуто. Большинство статей этой группы ученых временно отозвали — но поиски продолжают другие команды по сей день: это видно на сайте clinicaltrials.gov. В ряде исследований удалось уменьшить объем повреждения сердца мыши после инфаркта инъекцией особых стволовых клеток.
image004.jpg) |
| Срезы сердца мышей после инфаркта. Розовое — здоровые участки. Истонченное синее — умершая ткань. Справа меньше всего умершей ткани — в это сердце ввели стволовые клетки, запрограммированные так, что они выделяют особые молекулы. Работа корейских ученых от 2019 года. |
Клетки пациента чаще всего получают из мочи, кусочка верхнего слоя кожи или иным доступным способом. А в 2008 году в Европе получилось сделать настоящие клетки сердца из человеческого волоса! В открытом доступе есть полуминутная демонстрация их сокращений.
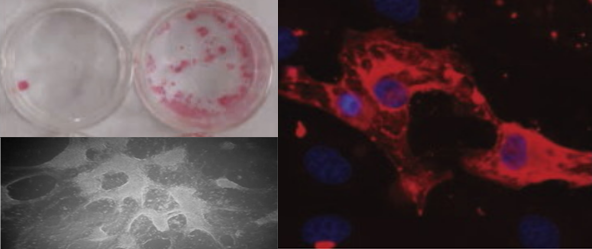 |
| Слева вверху чашки Петри с клеточными культурами через 17 дней после начала перепрограммирования (розовым окрашены те, у которых есть белок, отвечающий за более эффективное перепрограммирование). Слева снизу — готовый слой клеток сердца, клетки сокращаются как в живом сердце. Справа — они же под микроскопом |
После того, как из iPSC получаются зрелые клетки, нужно создать объемную структуру — пересадить их на 3D-каркас. Как правило, для этого используют синтетические материалы, но в 2019 году опубликованы иллюстрированные результаты международного проекта с участием сотрудника биологического факультета МГУ Вячеслава Иваненко. Ученые использовали в качестве каркаса морские губки: клетки сердца на них начали сокращаться уже через сутки после высаживания!
А коллектив авторов из Рязани опубликовал в журнале «Наука молодых» результаты исследований клеток кровеносных сосудов, полученных из iPSC. Это дает возможность наглядно изучать стенки сосудов — ведь мы не можем увидеть их у живого человека. Например, ранее удалось выявить молекулярные признаки повреждения сосудов, изучить сосуды при сахарном диабете.
image006.jpg) |
Слева — плоская культура клеток стенки сосуда. |
Ученые МФТИ за последние годы доказали, что можно проверять токсичность и связанные с сердцем побочные эффекты препаратов с помощью моделей, созданных при помощи iPSC. Так, удалось проверить циклофосфамид, лидокаин, эритромицин и изучить механизмы возникновения аритмий.
Мозг: синдром Дауна, болезнь Альцгеймера, болезнь Паркинсона
Ученые МГУ в 2016 году использовали технологию iPSC для изучения механизмов того, как у людей с синдромом Дауна развивается болезнь Альцгеймера. Сразу несколько команд исследователей Московского университета совместно с центром Рогачева изучали этим методом болезнь Паркинсона.
Если донор клеток страдает болезнью Паркинсона, то метод позволяет получить нейроны с этой патологией и подобрать лекарство, которое будет эффективно именно для этого пациента.
image009.png) |
| Модель органа с сосудами, доставляющими ему кровь с кислородом. С ее помощью можно исследовать, насколько хорошо лекарство будет проходить в мозг из кровяного русла — ведь там есть барьер. (адаптировано из обзорной статьи ученых Нью-Йорка) |
Как стволовые клетки помогают изучить COVID-19
Совместная работа ученых США и Канады позволила подробно изучить течение коронавирусного поражения легких и нарушения газообменной функции с помощью технологии iPSC (что этичнее планируемого в Великобритании эксперимента). Метод позволяет продолжить поиски лекарственных средств и исследовать имеющиеся. Аналогично изучали действие COVID-19 на нервную ткань, чтобы объяснить механизм развития у пациентов неврологических симптомов. К нервной ткани также относится сетчатка глаза, поэтому в Тайвани создали однослойную культуру — модель сетчатки из iPSC, чтобы изучить, как вирус проникает в эти клетки.
 |
| Клетки легких, выращенные из iPSC. Слева — здоровые, справа — пораженные COVID-19 |
Органы из iPSC
Если можно выращивать из iPSC разные ткани и даже на объемных каркасах — можно ли выращивать из них целые органы? Оказывается, есть множество публикаций на этот счет. Например, в 2018 году в Челябинске вырастили похожие на зуб структуры из клеток, полученных из человеческой мочи. В перспективе это позволит имплантировать такие структуры на место удаленного постоянного зуба.
image011.png) |
| Фотографии развивающихся зубов под микроскопом (окрашены). Источник: studfile.net |
А в 2019 году ученые Гарвардского университета придумали метод создания кровеносных сосудов в полученных органах. Для этого при помощи 3D-чернил в органе создают каналы, которые могут извиваться и разветвляться, как настоящие сосуды. Затем чернила из образованных каналов вымывают — каналы остаются пустыми — и ткань немедленно подключают к похожей на кровь (то есть способной переносить кислород) среде. При этом все клетки искусственного органа остаются жизнеспособными!
 |
Слева: пипетка 2,5 мл, в ней около полумиллиарда клеток. |
Вечная молодость — реальна?
Если ученые уже научились омолаживать клетки, то почему нельзя омолодить всего человека? Дело в том, что наш организм состоит по большей части из уже зрелых клеток.
Из одной клетки, образовавшейся в результате слияния яйцеклетки и сперматозоида, в процессе деления сначала получается «шарик из клеток», потом зародыш, который развивается в младенца и появляется на свет. Дальнейший рост ребенка также происходит за счет деления клеток.
Клетки, которые способны делиться — это «клетки-дети». Но большая часть клеток взрослого человека — уже «состоявшиеся». Мы можем взять несколько, сделать их «младенцами», перепрограммировать, снова вырастить и исследовать. Но даже если бы получилось все клетки человека вернуть в младенческое состояние — получился бы не младенец, а «шарик из клеток», какой был на начальных этапах развития под сердцем матери — только большого размера.
Этично ли?
Существует расхожее заблуждение, будто для получения стволовых клеток нужны человеческие эмбрионы. Выше мы уже опровергли это. А как насчет других этических вопросов?
В «Основах социальной концепции Русской Православной Церкви» стволовые клетки не упоминаются — однако есть положения касательно клонирования. Так, в разделе «Биоэтика» читаем:
«клонирование изолированных клеток и тканей организма не является посягательством на достоинство личности и в ряде случаев оказывается полезным в <…> медицинской практике»
Кроме того, с появлением iPSC часть исследований с участием лабораторных животных переквалифицировались на новые клеточные модели. Так что технология iPSC скорее решает этические трудности, чем создает их.









Screen-2021-05-20_10-46-44.jpg)